Giới thiệu
Trong hóa học vô cơ, nhiều hợp chất có khả năng phân hủy sinh ra khí oxi, được ứng dụng trong cả học tập lẫn đời sống. Một phản ứng tiêu biểu là KMnO4 ra O2, thường được sử dụng để điều chế oxi trong phòng thí nghiệm. Đây là kiến thức quan trọng, thường xuyên xuất hiện trong các đề thi và cũng có giá trị thực tiễn.
Phương trình hóa học KMnO4 ra O2
Khi đun nóng kali pemanganat (KMnO4), muối này sẽ bị phân hủy tạo thành muối mangan khác, đồng thời giải phóng khí oxi:
![]()
- Chất tham gia: Kali pemanganat (rắn màu tím đen).
- Sản phẩm: Kali manganat (K2MnO4, màu xanh lục), mangan đioxit (MnO2, rắn nâu đen) và khí oxi (O2).
- Hiện tượng: Khi nung, tinh thể KMnO4 chuyển dần sang màu xanh và nâu, khí oxi thoát ra có thể làm que đóm than hồng bùng cháy sáng.
Giải thích phản ứng KMnO4 ra O2
- Kali pemanganat là một chất oxy hóa mạnh. Khi bị nung nóng, nó mất đi sự bền vững, một phần Mn(VII) bị khử xuống Mn(IV) trong MnO2, một phần khác xuống Mn(VI) trong K2MnO4.
- Sự thay đổi số oxi hóa của mangan đi kèm với sự giải phóng O2, giúp phản ứng này trở thành một phương pháp kinh điển để điều chế oxi trong phòng thí nghiệm.
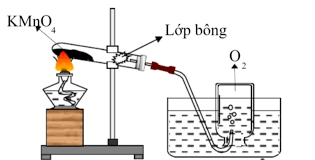
Ứng dụng của phản ứng KMnO4 ra O2
- Trong phòng thí nghiệm:
- Dùng để điều chế oxi với lượng nhỏ, phục vụ cho các thí nghiệm về tính chất của khí oxi.
- Giúp học sinh và sinh viên hiểu rõ bản chất phản ứng phân hủy.
- Trong thực tiễn:
- Oxi sinh ra được ứng dụng trong hàn cắt kim loại, y tế và nhiều ngành công nghiệp khác.
- KMnO4 còn có vai trò quan trọng trong khử trùng, xử lý nước và y học, dù mục đích chính không phải để sản xuất O2 quy mô lớn.

Lưu ý an toàn khi thực hiện phản ứng
- Cần đun nóng KMnO4 trong ống nghiệm chịu nhiệt, miệng ống nghiệm hướng ra xa người để tránh sự cố.
- Không hít trực tiếp khí thoát ra, mặc dù O2 không độc nhưng có thể gây cháy nổ nếu tiếp xúc với chất dễ cháy.
- KMnO4 là chất oxy hóa mạnh, phải bảo quản cẩn thận, tránh tiếp xúc với các chất khử hoặc chất dễ cháy.
Kết luận
Phản ứng KMnO4 ra O2 là một trong những phản ứng phân hủy quan trọng, được ứng dụng nhiều trong giáo dục và thực tiễn. Việc nắm vững phương trình, cơ chế và hiện tượng sẽ giúp học sinh không chỉ học tốt môn hóa học mà còn hiểu rõ cách điều chế khí oxi trong điều kiện an toàn.

