Giới thiệu
Trong hóa học vô cơ, phản ứng giữa oxit bazơ và oxit axit là một trong những nội dung cơ bản, thường gặp trong các bài tập và thí nghiệm. Một ví dụ điển hình chính là CaO + CO2, phản ứng tạo thành muối cacbonat quen thuộc. Đây là phản ứng vừa có giá trị lý thuyết, vừa mang tính ứng dụng cao trong đời sống và công nghiệp.
Phương trình hóa học CaO + CO2
Khi cho canxi oxit (CaO) tác dụng với khí cacbonic (CO2), phản ứng tạo ra muối canxi cacbonat (CaCO3):
![]()
- Chất tham gia: Canxi oxit (vôi sống) và khí cacbonic.
- Sản phẩm: Canxi cacbonat – chất rắn màu trắng.
- Hiện tượng: Xuất hiện chất rắn màu trắng không tan trong nước, đó là CaCO3.
Giải thích phản ứng CaO + CO2
- CaO là oxit bazơ, khi gặp CO2 (oxit axit) sẽ phản ứng để tạo thành muối trung hòa CaCO3.
- Đây là phản ứng điển hình của oxit bazơ + oxit axit → muối.
- CaCO3 thu được có tính bền, ít tan trong nước, là thành phần chính trong đá vôi, đá phấn và vỏ sinh vật biển.
Ứng dụng của phản ứng CaO + CO2
- Trong công nghiệp
- Phản ứng được ứng dụng trong sản xuất xi măng, vôi, gạch xây dựng.
- CaCO3 tạo ra có thể sử dụng làm chất độn trong công nghiệp nhựa, giấy, cao su.
- Trong đời sống
- Phản ứng CaO + CO2 giải thích quá trình tự nhiên khi vôi sống ngoài không khí lâu ngày sẽ bị “chết vôi” do hấp thụ CO2.
- CaCO3 còn được ứng dụng trong xử lý môi trường, khử chua đất nông nghiệp.
- Trong học tập
- Đây là ví dụ minh họa sinh động cho quy tắc phản ứng giữa oxit bazơ và oxit axit.
- Giúp học sinh hiểu sâu hơn về bản chất hóa học của muối cacbonat.
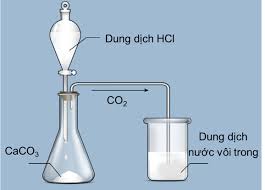
Lưu ý khi tiến hành phản ứng
- CaO có tính ăn mòn, khi tiếp xúc với nước tạo thành Ca(OH)2, có thể gây bỏng da. Cần sử dụng găng tay, kính bảo hộ khi làm thí nghiệm.
- CO2 là khí không màu, nặng hơn không khí, có thể gây ngạt trong không gian kín. Thí nghiệm phải thực hiện ở nơi thông thoáng.
Kết luận
Phản ứng CaO + CO2 → CaCO3 là một trong những phản ứng quan trọng trong hóa học và thực tiễn. Nó không chỉ xuất hiện trong sách giáo khoa mà còn gắn liền với nhiều ứng dụng trong đời sống hằng ngày, từ xây dựng, nông nghiệp đến công nghiệp sản xuất. Hiểu rõ phản ứng này giúp học sinh học tốt môn hóa và thấy được sự gắn kết giữa kiến thức khoa học với đời sống.

