Giới thiệu
Kali clorua (KCl) là một muối tan, phổ biến trong đời sống và công nghiệp. Trong hóa học, từ KCl có thể điều chế được HCl – một axit vô cơ quan trọng, ứng dụng rộng rãi trong sản xuất công nghiệp và nghiên cứu. Việc tìm hiểu phản ứng KCl ra HCl giúp làm rõ mối quan hệ giữa muối clorua và axit clohiđric, đồng thời củng cố kiến thức hóa học vô cơ.
Phương trình phản ứng KCl ra HCl
Để điều chế HCl từ KCl, người ta sử dụng phương pháp axit mạnh đẩy axit yếu hơn ra khỏi muối. Thông thường, dùng axit sunfuric đặc (H₂SO₄ đặc) tác dụng với kali clorua ở điều kiện nhiệt độ cao:
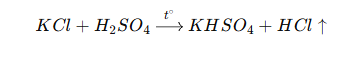
-
Chất tham gia:
-
KCl (rắn, muối tan)
-
H₂SO₄ đặc (axit mạnh, háo nước)
-
-
Sản phẩm:
-
KHSO₄ (muối axit, rắn)
-
HCl (khí)
-
Giải thích phản ứng
-
Axit sunfuric đặc có tính axit mạnh và tính háo nước, có thể tách ion Cl⁻ trong KCl để tạo khí HCl.
-
Khi đun nóng, khí HCl bay ra và có thể được dẫn vào nước để thu được dung dịch axit clohiđric.
-
Đây là phản ứng đặc trưng dùng trong công nghiệp để sản xuất HCl từ muối clorua.
Điều kiện phản ứng
-
Chất xúc tác: không cần xúc tác, nhưng phải dùng H₂SO₄ đặc.
-
Nhiệt độ: thường tiến hành ở nhiệt độ cao để phản ứng xảy ra hoàn toàn.
-
Môi trường: tiến hành trong bình kín, có ống dẫn khí để thu HCl sinh ra.
Ứng dụng thực tiễn
-
Sản xuất HCl công nghiệp:
-
Khí HCl sinh ra từ phản ứng trên được hấp thụ vào nước để tạo axit clohiđric tinh khiết.
-
Đây là phương pháp truyền thống trước khi có quy trình hiện đại sản xuất HCl từ clo và hiđro.
-
-
Trong nghiên cứu hóa học:
-
Thí nghiệm điều chế HCl trong phòng thí nghiệm thường sử dụng KCl và H₂SO₄ đặc.
-
-
Ý nghĩa học tập:
-
Minh họa quy tắc: axit mạnh đẩy axit yếu ra khỏi muối.
-
Giúp học sinh nắm vững phương pháp điều chế khí axit.

-
Bài tập minh họa

Kết luận
Phản ứng KCl ra HCl là một trong những phương pháp điều chế axit clohiđric từ muối clorua và H₂SO₄ đặc. Đây là phản ứng quan trọng trong phòng thí nghiệm, đồng thời từng được ứng dụng trong công nghiệp sản xuất HCl. Việc nắm vững cơ chế, điều kiện và ý nghĩa thực tiễn của phản ứng giúp củng cố kiến thức hóa học vô cơ và ứng dụng trong học tập cũng như thực tế.