Trong các thí nghiệm hóa học hoặc khi học chương trình hóa phổ thông, câu hỏi “ZnSO₄ có kết tủa không?” thường khiến nhiều người bối rối. Đây là một dạng câu hỏi kiểm tra khả năng vận dụng bảng tính tan và hiểu về tính chất của muối sunfat. Bài viết này Mẹo Vặt Cuộc Sống sẽ giúp bạn hiểu rõ bản chất của ZnSO₄, điều kiện để nó tạo kết tủa, cũng như những phản ứng minh họa cụ thể.
Tổng quan về ZnSO₄
ZnSO₄ là công thức hóa học của kẽm sunfat, một hợp chất vô cơ có dạng tinh thể không màu hoặc trắng, dễ tan trong nước.
-
Tên gọi: Kẽm sunfat
-
Công thức phân tử: ZnSO₄
-
Khối lượng mol: 161,44 g/mol (dạng khan)
-
Tính tan: Rất tan trong nước
-
Ngoại quan: Dạng tinh thể hoặc bột màu trắng, không mùi
Kẽm sunfat thường được dùng trong nhiều lĩnh vực: từ sản xuất phân bón, xử lý nước, làm nguyên liệu sản xuất pin, đến bổ sung kẽm trong chăn nuôi hoặc y tế.
ZnSO₄ có kết tủa không?
Câu trả lời là: Không – ZnSO₄ tan hoàn toàn trong nước, tạo dung dịch trong suốt, không có kết tủa.
Nguyên nhân:
Theo bảng tính tan:
-
Các muối sunfat (SO₄²⁻) của hầu hết các kim loại đều tan trong nước, trừ các trường hợp: BaSO₄, PbSO₄, SrSO₄, CaSO₄ (ít tan).
-
Zn²⁺ không thuộc nhóm tạo muối sunfat khó tan, do đó ZnSO₄ hòa tan dễ dàng và không tạo kết tủa trong dung dịch nước.
Khi nào ZnSO₄ tạo kết tủa?
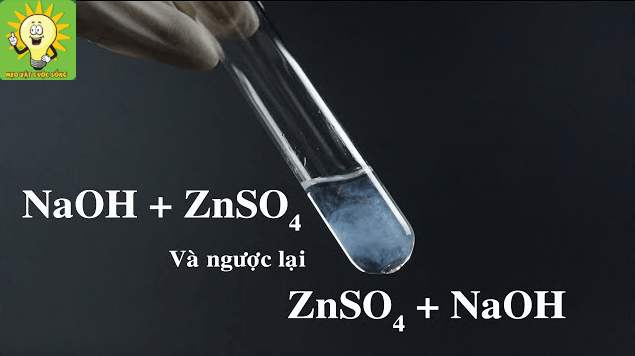
Mặc dù bản thân ZnSO₄ tan trong nước, nhưng khi nó tham gia phản ứng với một số dung dịch khác, các sản phẩm tạo ra có thể kết tủa. Một số trường hợp phổ biến:
-
Phản ứng với dung dịch NaOH
-
Phương trình:
ZnSO₄ + 2NaOH → Zn(OH)₂↓ + Na₂SO₄ -
Zn(OH)₂ là kết tủa trắng keo.
-
Khi cho dư NaOH, kết tủa Zn(OH)₂ tan tạo thành Na₂[Zn(OH)₄].
-
-
Phản ứng với dung dịch NH₃ (amoniac)
-
Ở lượng vừa phải: Zn²⁺ + 2NH₃ + 2H₂O → Zn(OH)₂↓ + 2NH₄⁺
-
Ở lượng dư: Zn(OH)₂ tan tạo phức [Zn(NH₃)₄]²⁺.
-
-
Phản ứng với muối cacbonat (Na₂CO₃, K₂CO₃)
-
ZnSO₄ + Na₂CO₃ → ZnCO₃↓ + Na₂SO₄
-
ZnCO₃ là kết tủa trắng.
-
Ứng dụng của ZnSO₄ trong thực tế

Dù không tạo kết tủa khi tan trong nước, ZnSO₄ lại có nhiều ứng dụng nhờ tính tan tốt và hoạt tính của ion Zn²⁺.
-
Nông nghiệp
-
Bổ sung kẽm cho đất và cây trồng, giúp tăng năng suất.
-
Thành phần trong phân bón vi lượng.
-
-
Y tế
-
Điều chế thuốc bổ sung kẽm.
-
Hỗ trợ điều trị tiêu chảy ở trẻ em.
-
-
Công nghiệp
-
Sản xuất pin, mạ kẽm.
-
Dùng trong xử lý nước để khử vi khuẩn.
-
Cách nhận biết ion Zn²⁺ trong dung dịch ZnSO₄
Để kiểm tra sự có mặt của Zn²⁺, bạn có thể thực hiện thí nghiệm nhỏ:
-
Dùng dung dịch NaOH hoặc NH₃ để tạo kết tủa trắng Zn(OH)₂.
-
Thêm NaOH dư hoặc NH₃ dư để quan sát kết tủa tan, xác nhận ion Zn²⁺.
Một số phản ứng minh họa
-
Với NaOH:
ZnSO₄ + 2NaOH → Zn(OH)₂↓ + Na₂SO₄ -
Với NH₃:
ZnSO₄ + 2NH₃ + 2H₂O → Zn(OH)₂↓ + (NH₄)₂SO₄ -
Với Na₂CO₃:
ZnSO₄ + Na₂CO₃ → ZnCO₃↓ + Na₂SO₄
Kết luận
-
ZnSO₄ tan hoàn toàn trong nước, không tạo kết tủa khi ở dạng dung dịch.
-
Kết tủa chỉ xuất hiện khi ZnSO₄ phản ứng với một số chất như NaOH, NH₃, Na₂CO₃… tạo ra hợp chất khó tan.
-
Hiểu rõ tính chất này giúp áp dụng trong phân tích hóa học và nhiều ứng dụng thực tế.

